La ataxia de Friedreich es un trastorno genético devastador que daña el sistema nervioso y el corazón, y para el cual hoy no existe cura. Sin embargo, un equipo multidisciplinario del CONICET y la UBA ha logrado un avance sin precedentes utilizando nanoanticuerpos derivados de llamas para reparar el defecto molecular dentro de las células humanas.
Afectando aproximadamente a una de cada 50 mil personas, la ataxia de Friedreich (AF) es una enfermedad degenerativa implacable. Su causa fundamental se esconde a nivel molecular: una alteración genética limita la producción de frataxina, una proteína vital que reside en las mitocondrias, las verdaderas «usinas de energía» de nuestras células. Al producirse de forma defectuosa o insuficiente, el sistema nervioso y el corazón sufren un daño progresivo.
Frente a este panorama, un equipo de científicos del CONICET y de la Universidad de Buenos Aires (UBA) acaba de publicar en la prestigiosa revista Communications Biology un hito terapéutico: desarrollaron nanoanticuerpos específicos capaces de ingresar a la célula y unirse a la frataxina defectuosa para estabilizarla.
De la llama al laboratorio
La clave de este descubrimiento tiene un origen peculiar. El equipo inmunizó a una llama en el INTA Castelar inyectándole la variante humana de la frataxina. El objetivo era aprovechar una característica única del sistema inmunológico de los camélidos: su capacidad para generar anticuerpos de cadena pesada, de los cuales se derivan los «nanoanticuerpos».
María Florencia Pignataro, primera autora del trabajo, explica por qué son tan especiales: «Son pequeñas moléculas que tienen la capacidad de penetrar membranas celulares, ubicarse en las mitocondrias y estabilizar proteínas defectuosas de frataxina. Constituyen una herramienta útil y versátil por su pequeño tamaño y alta afinidad».
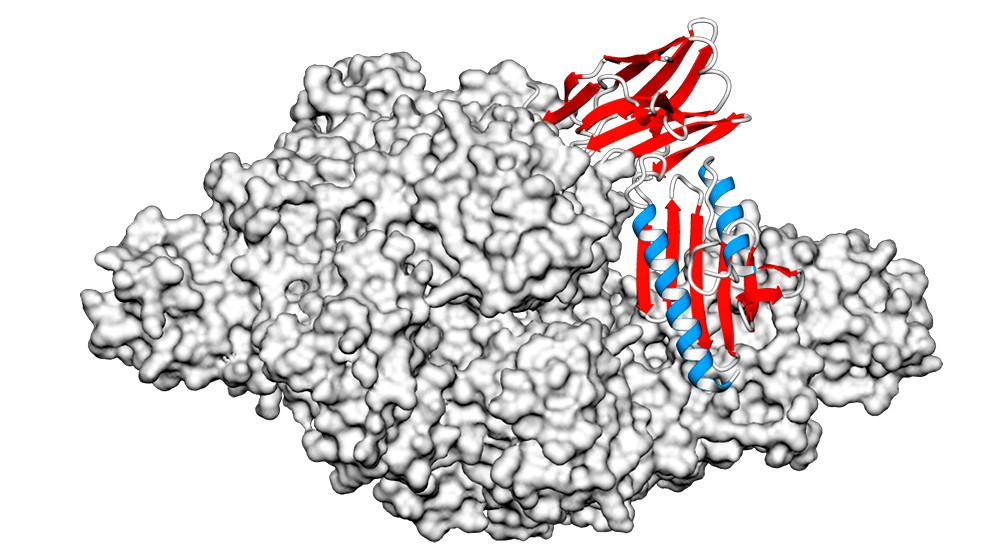
Al ser tan pequeños, estos nanoanticuerpos superan a los fármacos tradicionales. Itatí Ibañez, colíder del proyecto, subraya que un único vector de terapia génica podría transportar varios de ellos al mismo tiempo, lo que representa una ventaja clínica gigantesca frente a otras moléculas terapéuticas.
Reparar sin dañar
Uno de los grandes miedos al introducir agentes externos en las mitocondrias es alterar el frágil equilibrio de la célula. Sin embargo, Javier Santos, investigador de la UBA y colíder del avance, aporta un dato fundamental: la presencia de estos nanoanticuerpos no afecta la viabilidad ni la respiración celular. «Esta información es alentadora si pensamos en posibles terapias», destaca el científico.
El impacto de este desarrollo, que cuenta con el apoyo de biobancos hospitalarios (como el Hospital Italiano) y centros de investigación en España, ha cruzado fronteras. El laboratorio argentino recibió recientemente un importante subsidio internacional de la Alianza para la Investigación de la Ataxia de Friedreich (FARA) para acelerar sus estudios.
El próximo desafío es probar esta estrategia en modelos preclínicos, un paso vital antes de evaluar su seguridad y eficacia en pacientes reales. La ciencia argentina ha dado el primer paso firme para transformar una enfermedad incurable en una patología tratable.
Referencia:
Pignataro, M. F., Fernández, N. B., Garay-Alvarez, A., Pavan, M. F., Molina, R., Muñoz, I. G., … & Santos, J. (2026). Nanobodies as tools for studying human frataxin biology. Communications Biology.



